| بیکربنات سدیم | |||
|---|---|---|---|
 | |||
| |||
 | |||
| شناساگرها | |||
| شماره ثبت سیایاس | ۱۴۴-۵۵-۸ | ||
| پابکم | ۵۱۶۸۹۲ | ||
| کماسپایدر | ۸۶۰۹ | ||
| UNII | ۸MDF5V39QO | ||
| شمارهٔ ئیسی | ۲۰۵-۶۳۳-۸ | ||
| دراگبانک | DB01390 | ||
| KEGG | C12603 | ||
| MeSH | Sodium+bicarbonate | ||
| ChEBI | CHEBI:32139 | ||
| ChEMBL | CHEMBL۱۳۵۳ | ||
| شمارهٔ آرتیئیسیاس | VZ0950000 | ||
| کد اِیتیسی | B05,B05XA02 (WHO) QG04BQ01 | ||
| ۴۱۵۳۹۷۰ | |||
| جیمول-تصاویر سه بعدی | Image 1 | ||
| خصوصیات | |||
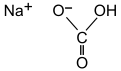
| فرمول مولکولی | NaHCO3 | ||
| جرم مولی | ۸۴٫۰۰۷ g mol−۱ | ||
| شکل ظاهری | White crystals | ||
| بوی | odorless | ||
| چگالی | ۲٫۲۰ g cm−۳[۱] | ||
| دمای ذوب | ۵۰ درجه سلسیوس (۱۲۲ درجه فارنهایت; ۳۲۳ کلوین) decomposes | ||
| دمای جوش | ۸۵۱ °C, 1124 K, 1564 °F | ||
| انحلالپذیری در آب | ۹ g/100 mL69 g/L (0 °C)[۲] ۹۶ g/l (20 °C)[۳] ۱۶۵ g/l (60 °C)[۳] ۲۳۶ g/L (100 °C)[۲] | ||
| انحلالپذیری | insoluble in اتانول | ||
| log P | -۰٫۸۲ | ||
| اسیدی (pKa) | ۱۰٫۳۲۹[۴]۶٫۳۵۱ (carbonic acid)[۴] | ||
| ضریب شکست (nD) | ۱٫۳۳۴۴ | ||
| داروشناسی | |||
| Routes of administration | Intravenous oral | ||
| ترموشیمی | |||
آنتروپی مولار استاندارد S | ۱۰۲ J·mol−۱·K−۱[۵] | ||
آنتالپی استاندارد تشکیل ΔfH | −۹۴۸ kJ·mol−۱[۵] | ||
یکربنات سدیم یا جوش شیرین با فرمول NaHCO۳ یکی از نمکهای سدیم در ترکیب با کربنیک اسید است که تنها یک هیدروژن اسیدی این ترکیب با سدیم جایگزین شدهاست. این ترکیب، بیبو و بیطعم است که کمی دارای خاصیت بازی است و به صورت پودر سپید یا بلورین است. بیکربنات جاذب رطوبت و بوگیر است.
این ترکیب ماده برای متخلخل کردن خمیر نان استفاده میشود و نیز برای کم کردن اسید معده و درمان سوزش آن به کار میرود.
محتویات
فرآوری
بیکربنات سدیم بیشتر به وسیلهٔ فرایند سالوی ساخته میشود که همان واکنش کلرید سدیم، آمونیاک و کربن دیاکسید در آب است که بیکربنات سدیم به صورت رسوب به دست آمده پس از صاف کردن و خشک کردن با حرارت به کربنات سدیم تبدیل خواهد شد. سالانه نزدیک به ۱۰۰۰۰۰ تن جوش شیرین فرآوری میشود. (سال ۲۰۰۱)[۶] همچنین میتوان با عبور دادن گاز از درون محلول جوشان کربنات سدیم خالص یا محلول هیدروکسید سدیم، بیکربنات سدیم را به شکل رسوب تهنشین شده به دست آورد.
ویژگیها
جوش شیرین در آب یک آمفوتر است. یعنی در آب میتواند به عنوان اسید یا باز رفتار کند. رفتار اسیدی آن به سبب وجود هیدروژن در ترکیبش است که در صنایع مختلف به عنوان آزادکننده کاربرد دارد.
حلالیت
در دمای معمولی ۱۰٫۳ گرم از این ماده در ۱۰۰ گرم آب حل میشود. اما در اتانول به مقدار کم محلول است.
کاربرد
بیشترین استفاده از بیکربنات سدیم در فرآوری انواع بکینگ پودر است.[نیازمند منبع] مقدار اضافی از خمیر جوش شیرین بطور مؤثر در پاک کردن و سائیدن سطوح میتواند استفاده گردد. استفاده از این ماده در ترکیب خمیر دندان به رفع تدریجی لکههای دندان و سفید شدن آنها کمک میکند.[نیازمند منبع] در صنایع غذایی، تولید نوشابههای گازدار به عنوان منبع، صنایع پاک کنندههای خانگی و در کپسولهای خاموش کننده آتش بکار میرود.[نیازمند منبع] همچنین به عنوان باز دارنده در مواد منفجره استفاده میشود. در صنعت نساجی برای عمل آوردن نخهای پشمی و ابریشمی استفاده میشود. همچنین میتواند به عنوان پاک کننده و ساینده ملایم در صورتی که ایجاد حساسیت نکند برای زیبایی پوست بکار رود. ضمن آنکه جوش شیرین به عنوان یک مکمل خوراکی در جیره غذایی دام و طیور میتواند در جهت جلوگیری از اختلالات متابولیکی و تغذیهای بکار برده شود.[نیازمند منبع]
کاربردهای بهداشتی
یکی دیگر از کاربردهای جوش شیرین در بهداشت بدن انسان است.[نیازمند منبع]
کاربردهای صنعتی
صنعت نساجی و دباغی یکی از بارزترین مصارف سدیم بی کربنات در تولید پارچههای پشمی و ابریشمی است. صنعت نساجی، از جوش شیرین برای رنگرزی و چاپ پارچه استفاده وسیعی میکند. صنعت دباغی نیز بی کربنات سدیم را بعنوان یک عامل خنثی کننده مواد رنگرزی در فراینده رنگ استفاده میکند.
صنعت پلیمر جوش شیرین استفاده گستردهای بعنوان کاتالیزور و تصفیه کننده در فرایند تولید پلیمرها و پلاستیکهای پیچیده دارد.
لاستیک و پلاستیک به دلیل اینکه بی کربنات سدیم، دی اکسید کربن آزاد میکند بنابراین بعنوان عامل فوم ساز در فرایند تولید لاستیک و پلاستیک استفاده میشود. دی اکسید کربن آزاد شده برای کنترل شکل محصولاتی که از لاستیک و پلاستیک ساخته میشود کاربرد دارد.
در صنعت تولید پودرهای آتشنشانی نیز کاربرد فراوانی دارد.
ایمنی
خوردن این ماده بیضرر است مگر اینکه به مقدار خیلی زیاد باشد. بوییدن آن ممکن است سبب سوزش بینی یا گلو شود. در اثر تماس با پوستهای حساس ممکن است باعث خارش یا سوزش پوست شود. در اثر تماس با چشم ممکن است سبب ایجاد سوزش و سرخی در چشم شود.
استفاده از جوش شیرین در پخت همه نوع نان و شیرینی مضر است.
کسانی که ناراحتی معده دارند، نبایستی از فراوردههایی که از جوش شیرین استفاده شده و به طور مشخص، نباید از نانهای پخته شده توسط جوش شیرین استفاده کرد. چرا که برای هضم غذا مضر است.[۷]
مصرف آرایشی
جوش شیرین یک لایه بردار قوی برای صورت است، همچنین از آن میتوان برای برطرف کردن بوی بد بدن نیز استفاده کرد اما شاید مهمترین اثر آرایشی-بهداشتی جوش شیرین درمان آفتاب سوختگی است که برای استفاده از آن کافی است در حمام آب گرم را باز کنید و نیم فنجان جوش شیرین به آن اضافه کنید تا یک لوسیون پوستی برای التیام آفتاب سوختگی داشته باشید.
منابع
- “Physical Constants of Inorganic Compounds”. CRC Handbook, p. 4-85.
- “Aqueous solubility of inorganic compounds at various temperatures”. CRC Handbook, p. 8-116.
- “Sodium Bicarbonate”. UNEP Publications.
- Goldberg, Robert N.; Kishore, Nand; Lennen, Rebecca M. “Thermodynamic quantities for the ionization reactions of buffers in water”. CRC Handbook. pp. ۷–۱۳٫
- Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. p. A23. ISBN ۰-۶۱۸-۹۴۶۹۰-X.
- Holleman, A. F. ; Wiberg, E.. Inorganic Chemistry. چاپ Academic Press: San Diego. ۲۰۰۱. شابک [[ویژه:منابع کتاب/ISBN: 0-12-352651-5|ISBN: ۰-۱۲-۳۵۲۶۵۱-۵]].
- Bishop, D. , J. Edge, C. Davis, and C. Goodman. Induced Metabolic Alkalosis Affects Muscle Metabolism and Muscle Metabolism and Repeated-Sprint Ability. Medicine and Science in Sports Exercise, Vol. 36, No. 5, pp. ۸۰۷–۸۱۳، ۲۰۰۴