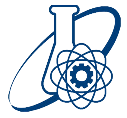
| آمونیوم دیکرومات | |
|---|---|
 | |
 | |
 | |
| شناساگرها | |
| شماره ثبت سیایاس | ۷۷۸۹-۰۹-۵ |
| کماسپایدر | ۲۳۰۰۲ |
| شمارهٔ یواِن | ۱۴۳۹ |
| شمارهٔ آرتیئیسیاس | HX7650000 |
| جیمول-تصاویر سه بعدی | Image 1 |
| خصوصیات | |
| فرمول مولکولی | (NH4)2Cr2O7 |
| جرم مولی | ۲۵۲٫۰۷ g/mol |
| شکل ظاهری | Orange-red crystals |
| چگالی | ۲٫۱۱۵ g/cm3 |
| دمای ذوب | ۱۸۰ درجه سلسیوس (۳۵۶ درجه فارنهایت; ۴۵۳ کلوین) decomposes |
| انحلالپذیری در آب | ۱۸٫۲ g/100ml (0 °C) ۳۵٫۶ g/100ml (20 °C) ۴۰ g/100ml (25 °C) ۱۵۶ g/100ml (100 °C) |
| انحلالپذیری | insoluble in استون soluble in الکل |
| خطرات | |
| MSDS | ICSC 1368 |
| GHS pictograms |      [۱] [۱] |
| GHS hazard statements | H272, H301, H312, H314, H317, H330, H334, H340, H350, H360, H372, H410[۱] |
| GHS precautionary statements | P201, P220, P260, P273, P280, P284[۱] |
| شاخص ئییو | ۰۲۴-۰۰۳-۰۰-۱ |
| طبقهبندی ئییو | ماده سرطانزا جهشزا Repr. Cat. 2 |
| کدهای ایمنی | R۴۵, R46, R60, R۶۱, R۲, R۸, R21, R۲۵, R۲۶, R۳۴, R42/43, R48/23, R50/53 |
| شمارههای نگهداری | S53, S45, S60, S61 |
| لوزی آتش | |
| دمای خودآتشگیری | ۱۹۰ °C |
آمونیوم دیکرومات (به انگلیسی: Ammonium dichromate)، یک ترکیب غیرآلی است که به دلیل استفادهاش در ایجاد آتشفشانهای رویمیزی گاهی با نام Vesuvian Fire (معنی Vesuvian: وابسته به کوه آتشفشان Vesuvius؛ آتشفشانی) نیز شناخته میشود. این ماده در مواد آتشزنه و در دوران نخستین عکاسی به کار رفته است.
محتویات
ساختار شیمیایی
فرمول شیمیایی آمونیوم دیکرومات (NH4)2Cr2O7 است. این ترکیب یک جامد یونی محسوب میشود که حاوی یونهای آمونیوم (NH4+) و دیکرومات (Cr2O72-) است[۲]. در ساختار بلوری، پیوندهای هیدروژنی به جهتدهی این یونها کنار هم کمک میکنند[۳]. به دلیل عدد اکسایش کروم که ۶+ است، آمونیوم دیکرومات یک عامل اکسنده، مادهای سمی و سرطانزا محسوب میشود
خواص فیزیکی
این ماده، همانند اکثر ترکیبهای یونی، در دمای معمولی جامد است و نقطه ذوب بالایی دارد. آمونیوم دیکرومات به شکل جامد نارنجی رنگ محلول در آب وجود دارد. انحلال آن در آب به دلیل جاذبههای یون – دوقطبی، پیوند هیدروژنی و همچنین نیروهای دوقطبی – دوقطبی (به دلیل قطبیت آنیون) صورت میگیرد.
خواص شیمیایی
واکنش کوه آتشفشان، معروفترین واکنش آمونیوم دیکرومات است که شامل تجزیهشدن مقداری از این ماده در اثر حرارت و انرژی اولیه است. معادله این واکنش گرماده را در زیر میبینید:
- (NH4)2Cr2O7(s) → Cr2O3(s) + N2(g) + 4H2O(f)
محصولهای این واکنش، بخار آب، گاز نیتروژن و جامد سبز رنگ کروم(III) اکسید است که در آب نیز نامحلول میباشد.
مانند مادهٔ آمونیوم نیترات شناخته شده، آمونیوم دیکرومات هم شامل یک اکسیدکننده (دیکرومات) و هم شامل یک کاهنده (آمونیوم) میباشد.[۴].
پانویس
- کاتالوگ آنلاین زیگما بدون تاریخ.
- Chemistry; Charles E. Mortimer; 6th Edition; Chapter7
- Keresztury, G. and Knop, O. (1982). “Infrared spectra of the ammonium ion in crystals. Part XII. Low-temperature transitions in ammonium dichromate, (NH4)2Cr2O7”. Can. J. Chem.: 1972–۱۹۷۶
- G.A.P. Dalgaard, A.C. Hazell and R.G. Hazell “The Crystal Structure of Ammonium Dichromate, (NH4)2Cr2O7” Acta Chemica Scandinavica A28 (1974) 541-545
منابع
Wikipedia contributors, “Ammonium dichromate,” Wikipedia, The Free Encyclopedia, http://en.wikipedia.org/w/index.php?title=Ammonium_dichromate&oldid=162611785 (accessed November ۸, ۲۰۰۷).