| آمونیاک | |||
|---|---|---|---|
| |||
| شناساگرها | |||
| شماره ثبت سیایاس | ۷۶۶۴-۴۱-۷ | ||
| پابکم | ۲۲۲ | ||
| کماسپایدر | ۲۱۷ | ||
| UNII | ۵۱۳۸Q19F1X | ||
| شمارهٔ ئیسی | ۲۳۱-۶۳۵-۳ | ||
| شمارهٔ یواِن | ۱۰۰۵ | ||
| KEGG | D02916 | ||
| MeSH | Ammonia | ||
| ChEBI | CHEBI:16134 | ||
| ChEMBL | CHEMBL۱۱۶۰۸۱۹ | ||
| شمارهٔ آرتیئیسیاس | BO0875000 | ||
| ۳۵۸۷۱۵۴ | |||
| ۷۹ | |||
| ۳DMet | B00004 | ||
| جیمول-تصاویر سه بعدی | Image 1 | ||
| خصوصیات | |||
| فرمول مولکولی | NH3 | ||
| جرم مولی | ۱۷٫۰۳۱ g/mol | ||
| شکل ظاهری | Colourless gas with strong pungent odour | ||
| چگالی | ۰٫۸۶ kg/m3 (1.013 bar at boiling point) ۰٫۷۳ kg/m3 (1.013 bar at 15 °C) ۶۸۱٫۹ kg/m3 at −۳۳٫۳ °C (liquid)[۱] ۸۱۷ kg/m3 at -80 °C (transparent solid)[۲] | ||
| دمای ذوب | −۷۷٫۷۳ درجه سلسیوس (−۱۰۷٫۹۱ درجه فارنهایت; ۱۹۵٫۴۲ کلوین) | ||
| دمای جوش | −۳۳٫۳۴ °C, 240 K, -28 °F | ||
| انحلالپذیری در آب | ۴۷% (۰ °C) ۳۱% (۲۵ °C) ۲۸% (۵۰ °C)[۳] | ||
| اسیدی (pKa) | ۳۲٫۵ (-۳۳ °C)[۴] ۱۰٫۵ (DMSO) | ||
| خاصیت بازی (pKb) | ۴٫۷۵ | ||
| ساختار | |||
| شکل مولکولی | Trigonal pyramid | ||
| لحظهٔ دوقطبی | ۱٫۴۲ D | ||
| خطرات | |||
| GHS pictograms |     [۵] [۵] | ||
| GHS hazard statements | H221, H280, H314, H331, H400[۵] | ||
| GHS precautionary statements | P210, P261, P273, P280, P305+351+338, P310[۵] | ||
| شاخص ئییو | ۰۰۷-۰۰۱-۰۰-۵ (anhydrous) ۰۰۷-۰۰۱-۰۱-۲ (solutions) | ||
| طبقهبندی ئییو | Toxic (T) Corrosive (C) Dangerous for the environment (N) | ||
| کدهای ایمنی | R۱۰, R۲۳, R۳۴, R50 | ||
| شمارههای نگهداری | (S1/2), S۹, S۱۶, S26, S36/37/39, S45, S61 | ||
| لوزی آتش |
| ||
| نقطه اشتعال | flammable gas (see text) | ||
| دمای خودآتشگیری | ۶۵۱ °C | ||
| محدودیتهای انفجار | ۱۵–۲۸٪ | ||
| آمریکا Permissible exposure limit (PEL) | ۵۰ ppm (25 ppm ACGIH – TLV; 35 ppm STEL) | ||
آمونیاک (به انگلیسی: Ammonia)با فرمول شیمیایی NH3، مهمترین ترکیب هیدروژنهٔ ازت (نیتروژن) است که در هوای شهرها و مجاورت توالتها وجود دارد. در طبیعت از تجزیهٔ مواد آلی ازت دار همچون اوره ادرار بهدست میآید.
آمونیاک سبب تحریکات دستگاه تنفسی، پوست و چشم شده و با آسیب رساندن به ششها در اثر مواجهه با حجم زیاد این گاز میتواند سبب مرگ شود.
رومیهای باستان آمونیوم کلرید را به عنوان پول و سپرده استفاده میکردند. آنها سنگ آمونیوم را از مکانی به نام پرستشگاه ژوپیتر یا همان لیبی جدید جمعآوری میکردند. اما آمونیاک به شکل نمک آمونیاک نخستین بار توسط شیمیدان جابر بن حیان (شیمیدان ایرانی) Geber در قرن ۸ شناخته شد.[۶]
محتویات
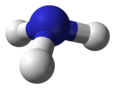
ساختار مولکولی
مولکول آمونیاک از یک اتم نیتروژن و سه اتم هیدروژن متصل به آن تشکیل شدهاست. با توجه به وجود یک جفت الکترون ناپیوندی بر روی نیتروژن، این مولکول ساختار هرم مثلثی دارد و زوایای پیوند کمتر از ۱۰۹ درجه هستند.[۷] مولکول آمونیاک یک مولکول قطبی است که میتواند با خودش و بسیاری مولکولهای دیگر، پیوند هیدروژنی برقرار نماید.
خواص فیزیکی
آمونیاک گازی است بیرنگ، با مزهٔ فوقالعاده تند و طعم حاد و زننده که اشکآور و خفهکننده است. گاز آمونیاک از هوا سبکتر بوده و به سهولت به مایع تبدیل میشود. آمونیاک درآب بسیار محلول بوده و در منفی ۷۷/۷ درجهٔ سانتیگراد منجمد شده و در منفی ۳۳/۳۴ درجهٔ سانتیگراد به جوش در میآید. وزن مخصوص محلول اشباع آمونیاک ۰/۸۸ گرم بر سانتیمتر مکعب است.
خواص شیمیایی
خصلت بازی
آمونیاک طبق نظریههای اسید و باز برونستد-لوری و لوویس، یک ترکیب بازی محسوب میشود. pH محلول آبی آن هم بیشتر از ۷ است که این واقعیت را آشکار میسازد. واکنش زیر، خصلت بازی مولکول آمونیاک را توضیح میدهد:[۸]
واکنش تفکیک بازی آمونیاک: (NH3(aq) + H2O(l) → NH4+(aq) + OH–(aq
واکنشهای دیگر
گاز آمونیاک قابل افروزش و حدود اشتعالش ۱۶–۲۵ درصد حجمی گاز آمونیاک در هوا است. حضور مواد نفتی و دیگر مواد افروختنی خطر آتشگیری را افزایش میدهد. مجاورت و تماس آمونیاک با نقره و جیوه تولید ” فورمینات نقره و جیوه ” میکند که موادی شدیداً قابل انفجار هستند. گاز آمونیاک در اثر گرمای از ۴۰۰ درجه به بالا تجزیه شده و تولید نیتروژن و هیدروژن میکند.
تولید
روشهای آزمایشگاهی
روشهای صنعتی
مهمترین روش صنعتی تولید آمونیاک، فرایند هابر نام دارد که شامل تهیة آمونیاک از عناصر سازندة آن میباشد. در این روش، گازهای نیتروژن و هیدروژن در دمای بالا و در فشار زیاد با هم واکنش میدهند و آمونیاک را تولید میکنند. کاتالیزگرهای مختلف هم به سهولت این واکنش کمک مینمایند.[۹]
کاربرد
از موارد استفادهٔ آمونیاک میتوان به استفاده در تهیهٔ کودهای شیمیایی، یخ سازی، اسید نیتریک، سایر ترکیبات نیتروژنه، مواد منفجره و نگهداری از مواد غذایی اشاره کرد.
یکی دیگر از کاربردهای آمونیاک میتوان به استفاده در رشته ورزشی وزنهبرداری و پاورلیفتینگ اشاره نمود. بوییدن این محلول باعث باز کردن عروق میشود و ورزش کار را تا حدودی عصبی میکند و در مهار کردن وزنه در مسابقات کمک میکند.
منابع
- Yost, Don M. (2007). “Ammonia and Liquid Ammonia Solutions”. Systematic Inorganic Chemistry. READ BOOKS. p. ۱۳۲٫ ISBN ۱-۴۰۶۷-۷۳۰۲-۶.
- Blum, Alexander (1975). “On crystalline character of transparent solid ammonia”. Radiation Effects and Defects in Solids. 24 (4): 277. doi:10.1080/00337577508240819.
- Perry, Dale L. ; Phillips, Sidney L. (1995). Handbook of inorganic compounds. CRC Press. p. ۱۷٫ ISBN ۰-۸۴۹۳-۸۶۷۱-۳.
- Perrin, D.D. , Ionisation Constants of Inorganic Acids and Bases in Aqueous Solution; 2nd Ed. , Pergamon Press: Oxford, 1982.
- کاتالوگ آنلاین زیگما ، تاریخ بررسی: June 6, 2011.
- http://www.irannh3.com www.irannh3.com
- Chemistry; Charles E. Mortimer; 6th Edition; Chapter9
- Chemistry; Charles E. Mortimer; 6th Edition; Chapter16
Chemistry; Charles E. Mortimer; 6th Edition; Chapter 23