| ظاهر | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
shiny grey جامد Spectral lines of Magnesium | |||||||||||||||
| ویژگیهای کلی | |||||||||||||||
| نام، نماد، عدد | منیزیم، Mg، ۱۲ | ||||||||||||||
| تلفظ به انگلیسی | /mæɡˈniːziəm/, mag-NEE-zee-əm | ||||||||||||||
| نام گروهی برای عناصر مشابه | فلزات قلیایی خاک | ||||||||||||||
| گروه، دوره، بلوک | ۲, ۳, s | ||||||||||||||
| جرم اتمی استاندارد | ۲۴٫۳۰۵۰ g·mol−۱ | ||||||||||||||
| آرایش الکترونی | [Ne] 3s2 | ||||||||||||||
| الکترون به لایه | ۲, ۸, ۲ | ||||||||||||||
| ویژگیهای فیزیکی | |||||||||||||||
| حالت | جامد | ||||||||||||||
| چگالی (نزدیک به دمای اتاق) | ۱٫۷۳۸ g·cm−۳ | ||||||||||||||
| چگالی مایع در نقطه ذوب | ۱٫۵۸۴ g·cm−۳ | ||||||||||||||
| نقطه ذوب | ۹۲۳ K, ۶۵۰ °C, ۱۲۰۲ °F | ||||||||||||||
| نقطه جوش | ۱۳۶۳ K, ۱۰۹۱ °C, ۱۹۹۴ °F | ||||||||||||||
| گرمای همجوشی | ۸٫۴۸ kJ·mol−۱ | ||||||||||||||
| گرمای تبخیر | ۱۲۸ kJ·mol−۱ | ||||||||||||||
| ظرفیت گرمایی | ۲۴٫۸۶۹ J·mol−۱·K−۱ | ||||||||||||||
| فشار بخار | |||||||||||||||
| |||||||||||||||
| ویژگیهای اتمی | |||||||||||||||
| وضعیت اکسید شدن | ۲, ۱ [۱] (strongly basic oxide) | ||||||||||||||
| الکترونگاتیوی | ۱٫۳۱ (مقیاس پاولینگ) | ||||||||||||||
| انرژیهای یونش (more) | نخستین: ۷۳۷٫۷ kJ·mol−۱ | ||||||||||||||
| دومین: ۱۴۵۰٫۷ kJ·mol−۱ | |||||||||||||||
| سومین: ۷۷۳۲٫۷ kJ·mol−۱ | |||||||||||||||
| شعاع اتمی | ۱۶۰ pm | ||||||||||||||
| شعاع کووالانسی | ۱۴۱±۷ pm | ||||||||||||||
| شعاع واندروالانسی | ۱۷۳ pm | ||||||||||||||
| متفرقه | |||||||||||||||
| ساختار کریستالی | hexagonal | ||||||||||||||
| مغناطیس | paramagnetic | ||||||||||||||
| مقاومت ویژه الکتریکی | (۲۰ °C) 43.9 nΩ·m | ||||||||||||||
| رسانایی گرمایی | (۳۰۰ K) 156 W·m−۱·K−۱ | ||||||||||||||
| انبساط گرمایی | (۲۵ °C) 24.8 µm·m−۱·K−۱ | ||||||||||||||
| سرعت صوت (سیم نازک) | (دمای اتاق) (annealed) ۴۹۴۰ m·s−۱ | ||||||||||||||
| مدول یانگ | ۴۵ GPa | ||||||||||||||
| مدول برشی | ۱۷ GPa | ||||||||||||||
| مدول حجمی | ۴۵ GPa | ||||||||||||||
| نسبت پواسون | ۰٫۲۹۰ | ||||||||||||||
| سختی موس | ۲٫۵ | ||||||||||||||
| سختی برینل | ۲۶۰ MPa | ||||||||||||||
| عدد کاس | ۷۴۳۹-۹۵-۴ | ||||||||||||||
‘منیزیم فلزی است به رنگ سفید یا نقرهای با نماد Mg، عدد اتمی ۱۲، وزن اتمی ۲۴٫۳۰۵۰ و ساختار بلور آن شش گوش یا هگزاگونال متراکم است. نام منیزیم از واژه ی یونانی Magnesia حوضهای در Thessaly یا از نام شهر قدیمی Magnesia در آسیای صغیر گرفته شدهاست. منیزیم هشتمین عنصر فراوان در پوسته زمین و سومین عنصر فراوان و محلول در آب دریاست.
منیزیم در گروه دو (IIA) جدول تناوبی به عنوان فلز قلیایی خاکی قرار دارد.
محتویات
ویژگیهای منیزیم[۲]
منیزیم به عنوان سبکترین فلز صنعتی با ویژگیهای منحصر به فرد متالورژیکی، کاربردهای وسیعی در صنایع مختلف یافتهاست. علیرغم وجود محدودیتهای ذاتی در تولید و استفاده از منیزیم به دلیل این ویژگیها روز به روز به کاربرد این فلز در صنایع مختلف افزوده میشود. میتوان از ویژگیهای منحصر به فرد منیزیم موارد زیر را برشمرد:
- منیزیم با چگالی ۱٫۷ گرم بر سانتیمتر مکعب، سبکترین فلز با قابلیت تولید قطعات صنعتی میباشد. چگالی منیزیم ۳۰ درصد از آلومینیوم کمتر (چگالی آلومینیوم ۲٫۷ گرم بر سانتیمتر مکعب) و تنها ۲۰ درصد چگالی آهن است (چگالی آهن ۷٫۸ گرم بر سانتیمتر مکعب). این ویژگی منحصر به فرد جذابیت فراوانی برای استفاده از این فلز در تولید قطعات متحرک و صنعت حمل و نقل ایجاد کردهاست.
- همراه با چگالی پایین، آلیاژهای منیزیم استحکام قابل توجهی از خود نشان میدهند. این ویژگی سبب افزایش نسبت استحکام به وزن این فلز شدهاست. به عنوان مثال جهت تغییر جنس تیری ۱۰ کیلویی از فولاد، میتوان بدون تغییر چقرمگی از تیری منیزیمی با وزن ۳٫۸ کیلوگرم استفاده کرد. نسبت بالای استحکام به وزن سبب شده در بسیاری از قطعات مختلف صنایع هوایی و خودرو سازی از منیزیم استفاده شود. نمونه چنین قطعاتی پوسته جعبه دنده هلیکوپتر میباشد.
- از ویژگیهای دیگر آلیاژهای منیزیم میتوان به قابلیت جذب ارتعاشات توسط این فلز اشاره کرد. این ویژگی سبب شده استفاده از آلیاژهای منیزیم برای مدیریت ارتعاشات مخصوصاً در صنعت خودرو بسیار مورد توجه قرار گیرد. در مقایسه با آلیاژ آلومینیوم A356 با ضریب میرایی ۱٪ در تنش ۱ مگا پاسکال، برای آلیاژ AZ91 منیزیم این ضریب ۲۵٪ میباشد. در تنش ۱۰۰ مگا پاسکال این ضریب برای آلومینیوم A356 %۴ و برای منیزیم AZ91 %۵۴ میباشد.
- علاوه بر قابلیت میرایی ارتعاشات، منیزیم سپری قوی در برابر امواج الکترو مغناطیس نیز میباشد. دیوارهای ۱ میلیمتری از منیزیم به راحتی میتواند امواجی با شدتهای بالاتر از ۸۵ دسی بل را سد کند. از این ویژگی منیزیم برای تولید بدنه تلفنهای همراه، تجهیزات الکترونیکی، نظامی و تولید سیمهای انتقال اطلاعات پرتوان استفاده میشود.
- یکی دیگر از خصوصیات آلیاژهای منیزیم در مقایسه با آلومینیوم پایداری ابعادی در برابر تغییرات حرارتی میباشد. در منیزیم، پارامترهای مختلف خواص حرارتی مانند رسانایی پایینتر و گرمای ویژه بالاتر از آلومینیوم میباشد. از جمله فرایندهای تحت تأثیر خواص حرارتی ماشین کاری دقیق میباشد. آلیاژهای منیزیم حین گرم و سرد شدن سریع در فرایند ماشین کاری، تغییرات ابعادی کمی دارند. این ویژگی ماشین کاری دقیق این آلیاژها را سادهتر میسازد.
- منیزیم در مقایسه با آلومینیوم، سیالیت بالا در ریختهگری، نیاز به فشار کمتر در دایکست و عدم واکنش با فولاد در بوته و قالب میباشد. با در نظر گرفتن این مزایا میتوان برای دایکست قطعهای منیزیمی از دستگاههای دایکست با ظرفیت کمتر استفاده نموده و تعداد به مراتب بیشتری قطعه در قالبهای مشابه فولادی تولید کرد.
محدودیتهای منیزیم[۲]
با وجود ویژگیهای منحصر به فرد و جذاب آلیاژهای منیزیم، این آلیاژها محدودیتهای ذاتی به همراه دارند که استفاده از آنها را محدود ساختهاست. دانشمندان در تلاش هستند که با طراحی آلیاژهای جدید و فرآیندهای تولید نو آورانه بر این محدودیتها فائق آیند. افزایش مصرف روزافزون آلیاژهای منیزیم نشان از موفقیت دانشمندان در توسعه کاربرد آلیاژهای منیزیم و چیره شدن مزیتها بر محدودیتهای این آلیاژها دارد. بطور کلی میتوان محدودیتهای آلیاژهای منیزیم را در سه دسته طبقهبندی کرد:
۱_ ناهمسانگردی خواص مکانیکی، منیزیم با ساختار هگزاگونال از تقارن پایینی در مقیاس بلوری برخوردار است. چینش خاص صفحات بلوری در ساختار هگزاگونال سبب شده در صفحاتی خاص تراکم شبکه به مراتب از صفحات دیگر بالاتر باشد. این تفاوت تأثیر مستقیمی بر قابلیت حرکت نابجاییها در جهات مختلف میگذارد. به صورتی که در برخی صفحات و جهات (صفحات قاعدهای) نابجاییها به راحتی و با تنش برشی پایین قابلیت حرکت پیدا میکنند، درحالی که در سایر صفحات (مانند صفحات منشوری و هرمی) قابلیت حرکت نابجاییها به شدت محدود است. این نا یکنواختی سبب محدودیتهایی در تغییر شکل میشود. در اثر حرکت نابجاییها شبکه کریستالی داخل دانهها به سوی جهت اعمال نیرو چرخش میکند. در آلیاژهای منیزیم به دلیل حرکت اکثر نابجاییها در صفحات قاعدهای، چرخش کریستالی اکثر دانهها به سمت جهتی واحد خواهد بود (صفحه نرمال قاعدهها به سوی جهت اعمال نیرو میگردد). در نتیجه پس از تغییر شکل ماده، پلی کریستال حاوی دانههایی خواهد بود که همگی با هم، هم راستا شدهاند و ناهمسانگردی ساختار هگزاگونال داخل خود را به کل قطعه تعمیم دادهاند. به عنوان مثال ورقی از آلیاژ منیزیم با چنین جهت گیری بلوری حین کشش عمیق به راحتی در راستای صفحه نابجاییها حرکت کرده و تغییر شکل میدهد. اما تغییر شکل در ضخامت ورق که وابسته به حرکت نابجاییها در صفحات منشوری و هرمی است بسیار محدود بوده و لذا تغییر شکل در این راستا ممکن نبوده و ورق به سرعت پاره میشود. در شکل انتهای صفحه سیستمهای لغزش و سیستمهای دوقلویی ساختار هگزاگونال منیزیم قابل مشاهده است. علیرغم چنین محدودیت ذاتی، دانشمندان روشهای مختلفی برای کنترل این محدودیت پیشنهاد کردهاند. به عنوان مثال تغییر شکل در دمای بالا باعث نزدیک تر شدن تنش برشی بحرانی حرکت نابه جاییها در صفحات قاعدهای و غیر قاعدهای میشود. همچنین استفاده از عناصر آلیاژی که باعث تغییر نسبت ارتفاع به عرض شبکه در بلور هگزاگونال منیزیم میشوند نیز به عنوان راهی دیگر برای افزایش شکلپذیری آلیاژهای منیزیم مورد توسعه قرار گرفتهاست. در روش سوم برای افزایش شکلپذیری منیزیم با استفاده از تغییر شکلهای نامتقارن (مانند نورد نا متقارن ورق) از هم جهت شدن دانهها جلوگیری میشود. با وجود ارائه راهکارهای متفاوت عموماً این روشها هزینه تولید را به شدت بالا برده و توجیه اقتصادی برای تولید انبوه را برای کاربردهای معمول زیر سؤال میبرد. این محدودیت آلیاژهای منیزیم سبب شده بیش از ۹۰٪ قطعات صنعتی ساخته شده با این آلیاژها با روشهای ریختهگری تولید شود و عموماً از تغییر شکل این آلیاژها مگر در موارد خاص اجتناب شود.
۲_ برای افزایش خواص مکانیکی در کاربردهای صنعتی، منیزیم با عناصر دیگر مخلوط شده و آلیاژهای مختلف تولید میشود. در آلیاژهای متداول و پر کاربرد منیزیم، افزایش استحکام از طریق ایجاد رسوبات مختلف صورت میپذیرد. این مکانیزم افزایش استحکام برای کاربرد در دماهای پایین بسیار مؤثر میباشد. اما با افزایش دما این رسوبات در فاز زمینه حل شده و این آلیاژها در دماهای بالا به شدت استحکام خود را از دست میدهند. از این رو استفاده از این آلیاژها در دماهای بالا و در شرایط تغییر شکل خزشی به چالشی برای دانشمندان تبدیل شدهاست. برای این محدودیت هم چارههای مختلفی اندیشیده شدهاست. از جمله این راهکارها میتوان به تولید آلیاژهای خاص با رسوبات مقاوم به حرارت و تولید کامپوزیتهای پایه منیزیم با ذرات تقویت شده سرامیکی اشاره کرد. در حال حاضر آلیاژهایی با مقاومت خزشی مناسب در دمای حداکثر ۴۰۰ درجه سانتی گراد ابداع شده و به صورت صنعتی مورد استفاده قرار گرفتهاست.
۳_ سومین محدودیت قابل ملاحظه منیزیم واکنش پذیری بالای این فلز میباشد. منیزیم با الکترونگاتیویته۳۱/۱ تقریباً قابلیت الکترون دهندگی به همه فلزات را دارا میباشد. از این رو در تماس با آنها پیل الکترو شیمیایی تشکیل شده، منیزیم خورده شده و فلز دیگر محافظت میشود. این خاصیت منیزیم برای تولید آندهای فدا شونده به نحو احسن استفاده میشود. اما در کاربردهای صنعتی، خوردگی بالا به عنوان محدودیت در کاربرد در نظر گرفته میشود. برای این محدودیت نیز راهکارهای متعددی بر پایه آلیاژ سازی و اصلاح ریز ساختار پیشنهاد شدهاست. لازم است ذکر شود که خوردگی سریع منیزیم در برخی کاربردها به عنوان مزیت نیز شناخته میشود. برای مثال از برخی از آلیاژهای منیزیم برای تولید استنتهای زیست تخریب پذیر برای درمان رگهای گرفته شده قلب استفاده نمود. این نوع از استنتها نیازی به جراحی مجدد برای خارج کردن نداشته و در مدتی کنترل شده به تدریج در محیط بدن حل میشوند.
در دماهای بالا واکنش پذیری بالای منیزیم بصورت احتراق در دمای پایینتر از دمای ذوب خود را نشان میدهد. این مسئله نیز در کاربرد و تولید قطعات منیزیمی موانعی ایجاد کردهاست. به عنوان مثال تا سال ۲۰۱۵ استفاده از قطعات منیزیمی داخل کابین هواپیماهای مسافربری ممنوع بودهاست. با این وجود، با پیشرفت تکنولوژی و معرفی آلیاژهای جدید مقاوم به احتراق، این ممنوعیت مطلق برداشته شده و به جای آن لزوم رعایت استاندارد جدید و مقاومت در آزمایشات سخت گیرانه جایگزین شدهاست. در فرآیندهای تولیدی مانند ریختهگری که ایجاد مذاب منیزیم اجتناب ناپذیر است نیز روشهای متعددی برای کنترل احتراق مورد استفاده قرار میگیرد. از جمله این روشها میتوان به استفاده از فلاکسها (عموما نمکهای کلریدی و فلوریدی) و گازهای محافظ اشاره کرد
تولید منیزیم
تولید منیزیم از آب دریا
در روش تولید منیزیم از آب دریا، منیزیم به صورت هیدروکسید رسوب کرده و بوسیله واکنش با اسید کلریدریک، به کلرید منیزیم تبدیل میشود. کلرید منیزیم بوسیله تبخیر محلول، بازیافت شده و فلز منیزیم بوسیله الکترولیز نمک مذاب بدست میآید.
فرایند الکترولیت
اولین مرحله از این فرایند فراهم کردن کلرید منیزیم-که بطور جزئی دهیدراته شده- یا کارنالیت دهیدراته میباشد. تغذیههای سلول صنعتی شامل مخلوطی از کلرید منیزیم دهیدراته، کلرید منیزیم جزئی دهیدراته شده یا کارنالیت دهیدراته میباشد.
کلرید منیزیم دهیدراته شده بوسیله یکی از این دو روش فراهم میشود: کلریده کردن اکسید منیزیم یا دهیدراته کردن آب نمک کلرید منیزیم.
سلول الکترولیتی شامل مخزن آجر کاری شدهاست که به محفظههای کاتد و آند تقسیم میشود. آند گرافیتی هوا- خنک شونده یا آب- خنک شونده و کاتد فولادی در الکترولیت متشکل از کلریدهای قلیایی با افزودنی کلرید منیزیم، غوطه ور میشوند. دمای کاری بین ۷۵۰–۶۸۰ درجه سانتی گراد است. کلرید منیزیم در سلول الکترولیتی مطابق واکنش زیر تجزیه میشود:[۳]
MgCl_2→Mg+Cl_2
منیزیم فلزی در کاتد تشکیل شده (روشنتر از الکترولیت است) و شناور میشود تا در قسمت کاتد جمع شود. کلر که محصول فرعی این فرایند است در آند جمع میشود.
در کشورهایی که انرژی الکتریکی ارزان است و بازار مصرف پایداری وجود دارد، تولید به روش الکترولیز به صرفه است. این مقرون به صرفه بودن زمانی بیشتر است که کلرید منیزیم مورد نیاز از منبعی مثل آب دریا تأمین شود.[۴]
فرایند احیای سیلیکوترمی
منیزیم طی فرایند سیلیکوترمی در دماهای بالا با فروسیلیسیم کاهش یافته و کریستالهای منیزیم تشکیل میشوند. این فرایند شامل احیای اکسید منیزیم مذاب بوسیله فروسیلیسیم تحت فشار گاز در دمای حدود ۱۴۰۰ درجه سانتی گراد میباشد. منیزیم فلزی در این فرایند تشکیل شده، تبخیر میشود و سپس دور از منطقه گرم تقطیر میگردد. منیزیم تقطیر شده دارای خلوص ۹۹٫۸٪ است و سپس مجدداً ذوب و ریختهگری میشود.[۵]
حال در انتهای این بخش به دلیل موضوعیت این فرایند در گزارش تهیه شده و استفاده از این روش به عنوان تنها روش تولید منیزیم در کشور، لازم دیده میشود که این فرایند را به طور خلاصه شرح دهیم.
به صورت کلی این فرایند از ۴مرحله اصلی و چندین مرحله کنترلی تشکیل شدهاست که در ادامه به آنها پرداخته میشود.
واحد کلسیناسیون
در ایتدا این بخش سنگهای دولومیت استخراج شده پس از دپوسازی به واحد کنترل منتقل شده و میزان خلوص منیزیم در آن مورد بررسی قرار میگیرید، پس از تأیید شدن سنگهای استخراجی، این سنگها را غربال کرده و از لحاظ ابعادی بهینه میگردند. سپس به منظور افزایش خلوص منیزیم موجود در دولومیتهای استخراجی و آمادهسازی برای تحویل به بخش احیا، سنگها را وارد کورهٔ دوار میکنند، در این بخش سنگها موجود در دما ۱۲۰۰درجه سلسیوس قرار گرفته و گاز دیاکسید کربن خود را همانطور که در معادله زیر به آن اشاره شدهاست از دست میدهند.
(MgCO_3.CaCO_3 (solid)+Q→MgO.CaO(solid)+2CO_2+O_2(g
پس گذر سنگهای مورد نظر از این بخش، سنگهای خاکستری اولیه به رنگ سفید درآمده و به بخش بعدی منتقل میگردد. لازم است ذکر شود که گاز خروجی از این کوره حاوی مقادیر قابل توجهی از آب و دیاکسید کربن میباشد که بررسی چگونگی استفاده از ضایعات تولیدی خود میتواند مفصلاً مورد بررسی قرار گیرد.
واحدآسیا و بریکت سازی
در این بخش دولومیتهای کلسینه شده به منظور آمادهسازی برای تحویل به بخش احیا به نسبتهای مشخصی با فروسیلیس(۷۵درصدکربن) و فلورین مخلوط میگردد، این مواد مخلوط شده سپس وارد آسیا گشته و در چندین مرحله پودر میشوند.
پس از مراحل فوق موادآسیا شده به منظور بهینهسازی شکلی و ابعادی، به شکل بریک درآورده شده و در محفظههایی برای انتقال به مرحله بعد نگهداری میشوند.
واحد احیاء منیزیم
در این مرحله بریکتها را درون محفظه ای استوانه ای شکل که ریتورت نام دارد، شارژ میکنند. پس شارژ ریتورتها، داخل محفظه ریتورتها توسط دو پمپ خلأ در دو مرحله تخلیه میشود، اولین پمپ فشار داخل ریتورت را به فشاری در حدود ۱۱۰ پاسکال رسانده و دیگر این فشار را به حدود ۱۰الی ۵ پاسکال میرساند. ابن فرایند احیاء حدود ۱۰ ساعت به طول میانجامد که در طی آن منیزیم موجود در بریکتها توسط فروسیلیس احیاء شده و به سمت دیگر ریتورت که کندانسور تعبیه شده و فشار کمتری دارد منتقل میشود. سپس منیزیم در محفظهٔ ابتدایی ریتورت که محفظه چگالش نام دارد از گاز به جامد تبدیل میشود که به اصطلاح آن را کرون یا تاج منیزیم مینامند. بقیه مواد داخل ریتورت که بریکت سوخته نام دارند نیز از ریتورتها تخلیه و در به عنوان دور ریخت جمعآوری میشود. فرایند گفته شده در بالا در معادله زیر خلاصه میشود.
(۲MgO.CaO(s)+Si(Fe)(s) →۲Mg(g) +CaO.SiO_2(s) +Fe(s
واحد ریختهگری
کرونها تولید شده در مرحله قبل، به خلوص مورد نظر رسیدهاند ولی به دلیل اشکال و اندازه غیر استاندارد و بد کرونهای سرد شده نیاز است که این کرونها در کورههای دوباره ذوب شده و برای بستهبندی و فروش به شمش تبدیل شوند.[۶]
مشخصات شیمیایی
منیزیم در حالت پودری، گرم میشود و زمانی که در معرض هوا قرار میگیرد، آتش گرفته و با شعلهای به رنگ سفید میسوزد. این فلز قلیایی خاکی عمدتاً به عنوان یک عامل آلیاژ دهنده برای ساخت آلیاژهای آلومینیوم – منیزیم استفاده میشود. این عنصر بصورت سه ایزوتوپ یافت میشود: ۲۶Mg, ۲۵Mg, ۲۴Mg که همهٔ این ایزوتوپها به مقادیر زیاد یافت میشوند. حدود ۷۹٪ از منیزیم نوع ۲۴Mg است.
کانیهای منیزیم
اگر چه منیزیم در ۶۰ کانی یافت میشود اما این عنصر در ذخایر بزرگ منیزیت، دولومیت، بروسیت، کارنالیت، الیوین و سیلیکاتهای منیزیم پتانسیل اقتصادی دارند، یافت میشود.
کاربردهای عمده
کاربردهای منیزیم در صنایع مختلف به شرح زیر است:
- دیرگداز
- آلیاژ
- تولید فلز منیزیم
- داروسازی
- سولفور زدایی و نودولی شدن در صنعت آهن و فولاد
- کاربردهای شیمیایی
- اکسید منیزیم
- کربنات منیزیم
- بی سولفید منیزیم
- سولفات منیزیم
- کلرید منیزیم
- هیدروکسید منیزیم
- منیزیای پختهشده
- مکمل غذای حیوانات
کاربرد آلیاژهای منیزیم
آلیاژهای منیزیم به دلیل دارا بودن استحکام ویژه بالا جایگزین مناسبی برای فولاد و آلومینیوم برای استفاده در قطعات سبک در صنایع اتومبیل و الکترونیک میباشند که این موضوع باعث افزایش تقاضای این آلیاژ شدهاست. البته ورقهای منیزیمی در دمای پایین تغییر شکل بسیار کمی دارند، که باعث محدودیت شدید کاربرد آنها شدهاست. این شکلپذیری کم ناشی از غالب بودن سیستم لغزش قاعدهای آن در تغییر شکل است که در قطعات کارشده این بافت قاعدهای بسیار شدید میباشد. شکلپذیری ورقهای منیزیم بوسیلهٔ کاهش شدت بافت قاعدهای میتواند بهبود یابد[۷][۸][۹] از این رو تلاشهای زیادی برای کاهش این شدت به منظور بهبود شکلپذیری آن انجام شدهاست. ا فزودن عناصر آلیاژی مانند عناصر نادر خاکی و لیتیوم یک روش مؤثر برای تضعیف بافت قاعدهای است با این حال اضافه کردن این عناصر گرانقیمت، هزینهٔ تمام شده قطعه را افزایش میدهد؛ بنابراین نیاز به کنترل و کاهش بافت قاعدهای بوسیلهٔ به کاربردن تکنیکهای فرآیندهای تولید میباشد. در سالهای اخیر فرایندهایی مانند نورد نامتقارن،[۱۰] نورد متقاطع،[۱۱] خم کاری تکراری تک جهته،[۱۲] خم کاری تکراری، نورد کانال زاویهای با مقطع یکسان، شکل دهی غلطکی موجی، آنیل با دمای بالا قبل و بعد از نورد گرم، ترکیب نورد گرم و نورد دمای بالا[۱۳][۱۴] برای بهبود خواص ورقهای منیزیمی بکارگرفته شدهاست. در فرایند نورد به منظور جلوگیری از شکست و ایجاد ترک، پارامترهای فرایند برای آلیاژهای Mg باید به دقت کنترل شوند، دمای بالای نورد، نورد چند مرحلهای با کاهش ضخامت کم و آنیل کافی بین هریک از مراحل نورد در روش سنتی نورد به کار گرفته میشد.[۱۵] افزایش دمای فرایند برای شکلپذیری بهتر آلیاژ Mg به دو دلیل مفید است؛ اول این که سیستمهای لغزش غیر قاعدهای در دمای بالاتر فعال میشوند که این سیستمهای لغزش مستقل امکان شرکت در تغییر شکل را دارند[۱۶] و دلیل دوم تبلور مجدد دینامیکی میباشد که با افزایش دما، افزایش مییابد و باعث کاهش سختی ماده حین تغییر شکل میشود.[۱۷]
پزشکی
منیزیم معدنی برای قلب، عضله و کلیه مهم و مفید است. این ماده قسمتی از دندان و استخوان شما را میسازد. مهمتر از همه، این ماده آنزیمها را فعال میکند، به شما انرژی میدهد و به کارکردن بهتر بدن کمک میکند. این ماده همچنین استرس، افسردگی و بیخوابی را کاهش میدهد. ویتامین ب۶ به جذب منیزیوم مورد نیاز کمک میکند و با منیزیوم در بسیاری از کارها همکاری میکند. منیزیم در بسیاری از غذاها قابل دسترس است. اگرچه بسیاری از مردم در ایالات متحده منیزیم کافی از رژیم غذایی شان دریافت نمیکنند. قرصهای مغذی تنها میتواند به شما مقدار منیزیم دریافتی را نشان دهد. دانشمندان روشهای مختلفی برای مشخص کردن میزان منیزیم غذاهای متفاوت پیدا کردهاند. علاوه بر این بسیاری از غذاها به طور کامل تجزیه نشدهاند.
بیماریهای طبی مشخصی تعادل منیزیم بدن را بهم میزند. برای مثال همراه با استفراغ یا اسهال میتواند منجر به کمبود منیزیم به طور موقتی شود. بیماریهای معده و روده، دیابت. التهاب پانکراس، عملکرد بد کلیه و داروهای دیورتیک (ادرارآور) میتواند باعث کمبود طولانی مدت منیزیم شود. اگر مبتلا به یکی از بیماریهای ذکر شده هستید برای منیزیم مورد نیاز مصرفی تان، با پزشک معالج مشورت کنید.
کاربردها
مصرف کافی منیزیم میتواند در موارد زیر به شما کمک کند:
- جلوگیری از سخت رگی (تصلب شرایین)
- جلوگیری از حمله و سکته قلبی
- کاهش فشار خون
- کاهش چربی زرد (کلسترول) و تری کلیسرید خون
- تصحیح بی نظمیهای ضربان قلب
- توقف حمله حاد آسم
- کاهش میزان نیاز به انسولین در صورت دیابتی بودن
- جلوگیری از تشکیل سنگ کلیه
- درمان بیماری کرون
- درمان سر و صدای ناشی از کاهش شنوایی
- بهبود بینایی در صورت داشتن آب سیاه
- کاهش گرفتگی ماهیچه، زود پریشی، خستگی، افسردگی و احتباس مایع مرتبط با قاعدگی
- جلوگیری از عوارض جدی آبستنی مانند پره اکلامپسی و اکلامپسی
- نگهداری و تجدید سطح انرژی طبیعی بدن
- بهبود چگونگی خواب
- کاهش دل نگرانی و افسردگی
- کاهش آزارها و آثارها استرس
منابع غذایی
غنیترین منبع منیزیم شامل (TOFU)، آجیل (بادام، پسته، گردوی سیاه، …) تخم کدو، بادام زمینی، برگ سبر سبزیجات، غلات، گندم، آرد سویا، تخم کتان و ملاس ….
منابع خوب دیگر برای منیزیم آرد گندم، آرد جو، چغندر سبز، اسفناج، خرده گندم، حبوبات، جودوسر، موز، سیب زمینی (با پوست)، پسته. همچنین میتوانید منیزیم را از بسیاری گیاهان گونههای علفها و جلبکها به دست آورید، برای مثال: جلبک آگار، گشنیز، شوید، دانه غلات، شاهپسند، خردل خشک، ریحان، پودر کاکائو، تخم رازیانه، مرزه، تخم زیره، تخم ترخون، تخم مرزنجوش و تخم خشخاش.
اشکال دیگر
منیزیم به اشکال مختلف در دسترس است. بهترین فرم آن به صورت «قابل حل» عرضه میشود، که بدن راحتتر منیزیم این ترکیب را جذب میکند. این ترکیبات قابل حل به صورت کپسول ژلاتینی است. مکملهای توصیه شده منیزیم شامل سیترات منیزیم، گلوکونات منیزیم و لاکتات منیزیم است.
دیگر منابع هم خانواده منیزیم شامل شیر منیزیم (هیدروکید منیزیم) که اغلب به عنوان یک ملین یا آنتی اسید استفاده میشود، نمکهای «ایپوم» (سولفات منیزیم) که به عنوان یک ملین یا تقویت کننده استفاده میشود یا به وان حمام اضافه میشود. بعضی از اشکال منیزیم از طریق پوست قابل جذب است.
چگونگی مصرف
شما باید مقدار کمی از منیزیم را در روز با یک لیوان پر از آب مصرف کنید (تا باعث اسهال نشود) مقادیر توصیه شده روزانه به شرح زیر است:
- مردان بزرگسال بین ۱۹ تا ۳۴ سالگی: ۴۰۰ میلیگرم بعد از ۳۰ سالگی: ۴۲۰ میلیگرم
- زنان بزرگسال بین ۱۹ تا ۳۴ سال: ۳۱۰ میلیگرم بالاتر از ۳۰ سال ۳۲۰ میلیگرم
- پسران در سن ۱۴ تا ۱۸ سال: ۴۱۰ میلیگرم
- دختران در سن ۱۴ تا ۱۸ سال: ۳۶۰ میلیگرم
- بچهها در سن ۹ تا ۱۳ سال: ۲۴۰ میل گرم، بچهها در سن ۴ تا ۸ سال ۱۳۰ میلیگرم و بچههای سن ۱ تا ۳ سال: ۸۰ میلیگرم.
موارد احتیاط
اگر بیماری شدید کلیوی یا قلبی دارید بدون مشورت پزشک از مکملهای منیزیم استفاده نکنید.
مصرف بیش از حد شیر منیزیم (به عنوان مسهل یا آنتی اسید) یا نمکهای ایپسوم (به عنوان مسهل یا تقویت کننده) باعث میشود که شما مقادیر زیادی منیزیم هضم کنید، بویژه اگر مشکل کلیوی داشته باشید. مصرف زیاد منیزیم باعث ایجاد مشکلات جدی برای سلامتی و حتی مرگ میشود.
تداخلهای احتمالی
بعضی از غذاها، نوشیدنیها و داروها، باعث از دست دادن منیزیم بدن میشود.
سدیم (نمک)، کافئین، الکل، فیبر، ریبوفلاوین به میزان زیاد، انسولین دیورتیکها (ادرارآور) و دیجیتالها است.
بعضی از غذاها، نوشیدنیها و داروها، بدن را برای مصرف منیزیم مورد نیاز با مشکل و سختی روبرو میکند. اینها شامل کلسیم، آهن، منگنز، فسفر. روی و چربی است.
سوختن منیزیم
در گذشته منیزیم به عنوان لامپ پرنور فلاش عکاسی استفاده میشد. فلز منیزیم به راحتی اکسید شده و هنگام سوختن نور قوی را ساطع میکند به همین دلیل نیز از این عنصر به صورت پودر شده و خالص در فلاشهای عکاسی استفاده میکردند.
منیزیم ماده ای است که میتواند به عنوان گزینه ای مناسب برای سوخت بشر قرار گیرد. همانطور که گفته شد گرما ایجاد شده از سوختن هر کیلو زغال سنگ برابر ۳۰ مگاژول بوده و گرمای تولید شده از سوختن هر کیلو منیزیم برابر ۲۵ مگاژول است که اندکی از زغال سنگ کمتر است.
نکته حائز اهمیت آنجاست که ذخیره و انتقال منیزیم بر خلاف هیدروژن بسیار آسان میباشد.[۱۸]
منیزیم سوختی برای نیروگاههای حرارتی
درحال حاضر سوختهای فسیلی اصلیترین منبع تأمین انرژی نیروگاههای حرارتی میباشند و از طرفی دیگر این نیروگاهها بزرگترین تولید کنند کربن دیاکسید در جهان نیز میباشد حال اگر روزی بتوانیم منیزیم را به صورت فراوان تولید کنیم آنگاه میشود بروی این عنصر به عنوان منبعی جایگزین برای سوختهای فسیلی در این نیروگاهها حساب باز کرد که این کار میتواند به موثرترین روش برای کاهش دیاکسید کربن تبدیل گردد.
همانطور که میدانید از واکنش شیمیایی پودر منزیم و آب، هیدرژون تولید میشود که افزایش سرعت این واکنش رابطه مستقیمی با میزان کوچکی دانههای پورد منیزیم خواهد داشت. با سرعت گرفتن واکنش ذیل هیدروژن شروع به سوختن کرده به این صورت که هیدروژن خروجی با اکسیژن واکنش داده و از واکنش آنها بخار آبی حاصل میشود که به دلیل فشار و دمای بالایش قادر به چرخاندن توربین برای تولید الکتریسیته خواهد بود.
Mg + H2O → MgO + H2
محصول نهایی این واکنش منیزیم اکسید جامد و بخار آب میباشد که هیچکدام تخریب زیستمحیطی نخواهد داشت و منیزیم اکسید تولیدی را نیز میتوان به وسیله چرخهٔ بازیافت منزیم توسط لیزر خورشیدی دوباره به منیزیم خالص که به عنوان سوخت راکتور میباشد تبدیل کرد.[۱۹]
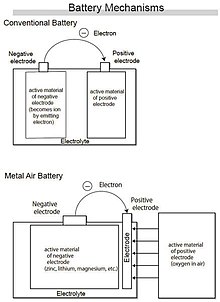
در باتریهای معمولی در الکترود منفی از مواد فعال الکترونده (این مواد عامل تولید الکتریسیته هستند) و در الکترود مثبت از مواد فعال الکترون گیرنده استفاده میشود. در Air Batteryها اکسیژن موجود در هوا به عنوان ماده الکترون گیرنده در الکترود مثبت قرار میگیرد و در الکترود منفی نیز مواد فعال الکترون دهنده قرار میگیرد. واضح است که به دلیل این که ماده خاصی در الکترود مثبت قرار نمیگیرد، چگالی انرژی در این باتریها نسبت به باتریهای متعارف دیگر به مراتب بالاتر است.
در باتری منیریم- هوا، منیزیم به عنوان مادهٔ فعال در الکترود منفی قرار میگیرد وقتی که منیزیم در الکترود منفی با اکسیژن در الکترود مثبت واکنش میدهد فرایند اکسید شدن رخ میدهد و انرژی الکتریکی تولید میشود و چیزی که باقی ماند اکسید منیزیم خواهد بود.
ما در اینجا به بررسی تفاوتهای بین موتور الکتریکی و اتومبیل با باتری منیزیم-هوا میپردازیم و هر دو طبقهبندی را با فرض آنکه قیمت منیزیم به حدی پایین بیاید که از آن بتوان به عنوان سوختی با صرفهٔ اقتصادی یاد کرد پیش میبریم.
بر اساس گزارش سازمان NEDO تا سال ۲۰۲۰ میلادی میزان مسافت طی شده توسط باتریهای یونی لیتیمی در یک دور شارژ کامل با وزنی حدود ۸۰ کیلوگرم به حدود ۲۰۰ کیلومتر خواهد رسید. حال با وزن ثابت میزان مسافت طی شده توسط باتری منیزیم- هوا، ۷ برابر خواهد شد و به طور معکوس با میزان مسافت طی شده برابر، وزن این باتری در مقایسه باتریهای یونی لیتیمی به یک هفدهم تقلیل مییابد؛ و این حقیقتی است که در آینده باعث افزایش استفاده از این باتریها خواهد شد. قضاوت در مورد فضای اشغال شده توسط باتریهای یونی لیتیمی بر اساس وزن این باتری تصویر روشنی را به ما نمیدهند و این به معنی است که فضای اشغال شده توسط این باتری خارج از دسترس نخواهد بود ولی بدیهی میباشد که باتریهای منیزیم هوا از لحاظ سایز نیز به مراتب استاندارد تر خواهد بود.
از منظری دیگر اکثر خودروها هنگام احتراق و تولید توان گاز دیاکسید کربن و دیگر گازهای مضر را تولید میکنند ولی باتریهای منیزیم-هوا از این نظر نیز سرآمد هستند ولی یکی از مشکلات اساسی این ماشینها سوخت گیری و شارژر طاقت فرسا این باتریها میباشد. به یاد دارید که یکی از مشکل اساسی خودروهای الکتریکی، زیر ساختهای ایستگاه سوخت گیری و شارژ این خودروها بود به طوری که نیاز بود تا این ایستگاهها در فواصل کمی نسبت به هم قرار گیرند تا بتوانند شرایط پیمودن مسیرها طولانی را فراهم سازند؛ ولی باتریها منیزیم-هوا همانند خودروهای الکتریکی نیازمند زیرساختهای وسیعی نمیباشند و منیزیم را میتوان به راحتی در فروشگاههای مختلف جایگزین منیزیم اکسید موجود در باتری نمود.
همانطور که میدانید از فعالیت باتری منیزیم-هوا، اکسید منیزیم تولید میشود و ایده بسیار کارامدی خواهد بود اگر فرایندی را تبعیه کرد که در آن بتوان منیزیم اکسید موجود در باتری را پس از جایگزین نمودن با پک منیزیمی جدید، در چرخه بازیافت توسط لیزر-پمپ شده- خورشیدی قرار داد.[۲۰]
از این گذشته باتریهای یونی لیتیمی، در زمینه تأمین مواد خام اولیه نیز با مشکلاتی رو به رو هستند. به طور معمول خودروها برای پیمودن مسافت ۵۰۰کیلومتری نیازمند توانی حدود ۱۰۰کیلووات ساعت هستند. حال به دلیل آنکه ظرفیت ویژه این عنصر برابر ۳٫۸۳A.h/g بوده و لتاژ خروجی این باتریها برابر ۳ ولت میباشد در نتیجه توانی برابر ۱۱٫۵ وات ساعت را به ازای هر گرم لیتیم تولید میشود که برای تأمین انژری فوق، ۸٫۷کلیلوگرم لیتیم نیاز خواهد بود (البته با فرض این که ۱۰۰٪ توان تولید توسط لیتیم قابل استفاده قرارگیرد). در حال حاضر ۹۰۰ میلیون خودرو در جهان در حال استفاده میباشد که میزان لیتیم مورد نیاز برای تجهیز این تعداد خودرو برابر ۷٫۸۰۰٫۰۰۰ خواهد بود و باتوجه به این که میزان ذخایر در حال دسترس فعلی لیتیم برابر ۴میلیون تن میباشد در نتیجه حتی اگر کل این مقدار در زمینه تولید خودرو مصرف شود با این حال این میزان از منابع کفاف تأمین این تعداد خودرو را نخواهد داشت. در حال حاضر سرانه تولید منابع لیتیم در جهان برابر ۲۵٫۰۰۰تن میباشد ولی انتظار میرود که با افزایش میزان تقاضا این مقدار در آینده به سرعت رشد کند و در حال حاضر نیز رقابتی در این زمینه در جهان الخصوص بین آمریکا جنوبی و کشور چین شروع شدهاست؛ ولی گفت این نکته لازم است که اگر باتریهای یونی لیتیمی فراگیر شوند در این صورت محدودیت ذخایری عنصر لیتیم نسبت به نفت خام بیشتر خواهد شد. همچنین گفته میشود که برای بازیافت لیتیم از باتریهای یونی لیتیمی مصرف شده بیشتر از هزینه تولید آنها به صورت معمول خواهد بود. آب دریا حاوی لیتیم میباشد و تحقیقاتی در زمینه استخراج لیتیم از آب دریا در دست انجام میباشد ولی در واقع میزان لیتیم موجود در آب دریا نسبت به میزان منیزیم بسیار ناچیز است به صورتی که در هر کیلوگرم آب دریا ۱٫۲۹g منیزیم یافت میشود که این میزان برای لیتیم به ۰٫۰۰۰۰۱gدر هر کیلوگرم آب دریا تقلیل مییابد از طرفی در حال حاضر هزینه استخراج لیتیم از آب دریا حدود ۱۰۰ الی ۲۰۰ دلار خواهد شد و نیاز است که این هزینه برای کارآمد شدن و مطرح شدن لیتیم به عنوان سوخت کاهش یابد.
‘ تحقیقات در مورد باتریهای فلز-هوا در منحصر به باتریهای منیزیم-هوا نمیشود بلکه از فلزاتی همچون آلومنیوم، لیتیم و سرب نیز در این باتریها استفاده میشود اگر چه که از امر این تحقیقات زمان زیاد نمیگذرد. لازم است ذکر شود که میزان چگالی انرژی باتریهای لیتیم-هوا از نوع منیزیمی این باتریها بیشتر است و در صورت استفاده از این لیتیم خروجی بیشتری نسبت به منیزیم خواهیم داشت؛ ولی همانطور که در مورد باتریهای یونی لیتیمی گفته شد مشکل کمبود منابع در مورد این باتریها نیز صادق است به صورتی که برای ساخت و تجهیز وسایل الکتریکی زیادی نیاز به لیتیم و ترکیبات مختلف آن خواهیم داشت؛ ولی میدانیم که سوخت باتری منیزیم-هوا رامی توان با هزیه کمی بازیافت کرد و از طرفی دیگر میزان ذخایر منیزیم نسبت به لیتیم به مراتب بیشتر است. به همین دلیل است که میتوان منیزیم را به عنوان سوختی مطمئن تر نسبت به لیتیم یاد کرد.
مادامی که ما بر خودروهای گازوئیلی تکیه میکنیم، نمیتوانیم روزی را تصور کنیم که خودروهای دیگری در شهرها تردد میکنند؛ با این حال که از عمر این ماشینها حدود۱۰۰ سال بیشتر نمیگذرد. به هر حال تصور میشود که در ۱۰۰ سال آینده خودروهایی با باتریهای منیزیم- هوا، جایگزین خودروهای فعلی شوند و صنعت خودرو سازی جهان را متحول سازند.
در پایان باید گفت که بشر در آینده به سمت سوختی باید برود که از لحاظ، در دسترس بودن و فروانی منابع غنی بوده و بتواند توان کارآمدی را با چگالی انرژی بالا و با صرفه اقتصادی تولید نماید و از طرفی دیگر بتواند نیاز آلودگیهای محیط زیستی بشر که ناشی از سوختن منابع انرژی میباشد را رفع کند. حال من حیث المجموع چرخه انرژی پاک جدید منیزیم و لیزر-پمپ شده- خورشیدی راه حلی است که میتواند کلیدی برای حل این مشکل باشد زیرا همانطور که در بخشهای گذشته به آن اشاره گردید این منبع ناتمام انرژی، با توجه به فراوانی و دانسیته انرژی بالا و پاک بودن چرخه تولید و استفاده میتواند به عنوان یکی از بهترین کاندیدها برای جایگزینی سوختهای فسیلی قرار گیرد.[۲۱]
منابع
- برنath, P. F., Black, J. H., & Brault, J. W. (1985). “The spectrum of magnesium hydride”. Astrophysical Journal 298: 375.
- A. Sadeghi et al. , Selected Topics On ADvanced Magnesium Technologies, First edit. Tehran: arvan, 1395.
- Pal, Uday B. ; Powell, Adam C. (2007). “The Use of Solid-Oxide-Membrane Technology for Electrometallurgy”. JOM. 59 (5): 44–۴۹٫ Bibcode:2007JOM….59e..44P. doi:10.1007/s11837-007-0064-x.
- Fulginiti, Daniele. Development of a thermal model for SPS modified for the production of bioimplants. Diss. Politecnico di Torino, 2016.
- Hoy-Petersen, N. ; et al. Magnesium. In Ullmann’s Encyclopedia of Industrial Chemistry, 5th ed. ; VCH: Weinheim, Germany, 1990; Vol. A15,p 559
- Winand, R. ; Van Gysel, M. ; Fontana, A. ; Segers, L. ; Carlier, J. C. Production of magnesium by vacuum carbothermic reduction of calcined dolomite. Trans. Inst. Min. Metall. , Sect. C: Miner. Process. Extract. Metall. 1990, 99 (May-Aug), C105-C112. See also: Li, Z. ; Dai, Y. ; Xue, H. Thermodynamic analysis and experimental test of magnesia vacuum carbothermic reduction. Youse Jinshu 2005, 57 (1), 56-59 (in Chinese)
- E. Yukutake, J. Kaneko, and M. Sugamata, “Anisotropy and Non-Uniformity in Plastic Behavior of AZ31 Magnesium Alloy Plates,” Mater. Trans., vol. 44, no. 4, pp. 452–۴۵۷, ۲۰۰۳٫
- K. Iwanaga, H. Tashiro, H. Okamoto, and K. Shimizu, “Improvement of formability from room temperature to warm temperature in AZ-31 magnesium alloy,” J. Mater. Process. Technol., vol. 155–۱۵۶, no. 1–۳, pp. 1313–۱۳۱۶, ۲۰۰۴٫
- X. Huang, K. Suzuki, A. Watazu, I. Shigematsu, and N. Saito, “Improvement of formability of Mg-Al-Zn alloy sheet at low temperatures using differential speed rolling,” J. Alloys Compd., vol. 470, no. 1–۲, pp. 263–۲۶۸, ۲۰۰۹٫
- Y. Chino et al., “Mechanical Properties and Press Formability at Room Temperature of AZ31 Mg Alloy Processed by Single Roller Drive Rolling. ,” Mater. Trans., vol. 43, no. 10, pp. 2554–۲۵۶۰, ۲۰۰۲٫
- Y. Chino, K. Sassa, A. Kamiya, and M. Mabuchi, “Microstructure and press formability of a cross-rolled magnesium alloy sheet,” Mater. Lett., vol. 61, no. 7, pp. 1504–۱۵۰۶, ۲۰۰۷٫
- B. Song, G. Huang, H. Li, L. Zhang, G. Huang, and F. Pan, “Texture evolution and mechanical properties of AZ31B magnesium alloy sheets processed by repeated unidirectional bending,” J. Alloys Compd., vol. 489, no. 2, pp. 475–۴۸۱, ۲۰۱۰٫
- X. Huang, K. Suzuki, and Y. Chino, “Influences of initial texture on microstructure and stretch formability of Mg-3Al-1Zn alloy sheet obtained by a combination of high temperature and subsequent warm rolling,” Scr. Mater., vol. 63, no. 4, pp. 395–۳۹۸, ۲۰۱۰٫
- Q. Miao, L. Hu, G. Wang, and E. Wang, “Fabrication of excellent mechanical properties AZ31 magnesium alloy sheets by conventional rolling and subsequent annealing,” Mater. Sci. Eng. A, vol. 528, no. 22–۲۳, pp. 6694–۶۷۰۱, ۲۰۱۱٫
- M. R. Ghandehari Ferdowsi, M. Mazinani, and G. R. Ebrahimi, “Effects of hot rolling and inter-stage annealing on the microstructure and texture evolution in a partially homogenized AZ91 magnesium alloy,” Mater. Sci. Eng. A, vol. 606, pp. 214–۲۲۷, ۲۰۱۴٫
- M. H. Yoo, “Slip, twinning, and fracture in hexagonal close-packed metals,” Metall. Trans. A, vol. 12, no. 3, pp. 409–۴۱۸, ۱۹۸۱٫
- S. M. Fatemi-Varzaneh, A. Zarei-Hanzaki, and H. Beladi, “Dynamic recrystallization in AZ31 magnesium alloy,” Mater. Sci. Eng. A, vol. 456, no. 1–۲, pp. 52–۵۷, ۲۰۰۷٫
- T. Rampe, A. Heinzel, and B. Vogel, J. Power Sources 86, 536 (2000).
- T. Yabe, S. Uchida, K. Yoshida, K. Ikuta, and T.Okamoto, in Proceedings of Fourth Intl. Symposiumon Beamed Energy Propulsion AIP Conf. Proc. 803, 21(2005).
- T. Yabe, K. Ikuta, C. Baasandash, R. Katano, S. Uchida, M. Tsuji, Y. Mori, J. Maehara, M. S. Mahmoud, and T. Toya, in Proceedings of Fourth Intl. Symposium on Beamed Energy Propulsion AIP Conf. Proc. 803, 447 (2005).
C. Hisatsune and T. Hagiwara, “Effect of beryllium onmagnesium and its alloys (3rd Report) Study on the ignition emperature of magnesium and its alloys” LightMetal (in Japanese) 14, 46 (1964)